Intertek为驼人集团颁发欧盟III类医疗器械MDR证书
近日,Intertek瑞典公告机构IMNB(NB 2862)依据欧盟医疗器械法规(MDR,EU 2017/745),为河南驼人医疗器械集团有限公司(以下简称“驼人集团”)颁发Ⅲ类产品麻醉包MDR认证证书。
自2020年双方启动MDD合作以来,Intertek与驼人集团携手走过五年历程,持续为其提供专业支持与技术赋能,助力集团旗下麻醉包、输注泵、压力传感器等数十项产品取得MDR认证证书,范围已全面覆盖Ⅰ类灭菌、Ⅱ类及Ⅲ类产品。此次Ⅲ类麻醉包MDR证书的获得,标志着双方合作再上新台阶,也为驼人集团进军欧盟市场注入强劲动力。
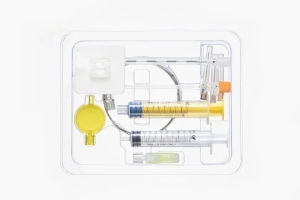
同心致远,互信共赢
五年来,Intertek与驼人集团紧密协作,逐步构建起覆盖多类别、多风险等级的欧盟准入“产品矩阵”,全面提升了驼人集团在国际医疗器械行业的品牌影响力与市场竞争力。
不仅如此,Intertek已助力驼人集团成功取得ISO 13485医疗器械质量管理体系认证及MDSAP证书,从体系建设到产品准入,为企业提供了全链条、一站式的国际化服务支持。
这些权威认证的叠加,不仅为驼人集团的国际市场拓展筑牢了质量根基,更彰显了Intertek在医疗器械认证领域的深厚积淀与专业实力,赢得了客户的高度认可与行业赞誉。
专业认证,权威护航
此次驼人集团III类麻醉包的MDR证书获取,是Intertek专业服务能力的又一力证。
作为欧盟医疗器械法规(MDR)下的权威公告机构(公告号:NB 2862),Intertek致力于为医疗器械企业提供覆盖产品全生命周期的“一站式”解决方案。
Intertek的MDR认证范围已经基本能够全面覆盖所有的医疗器械领域,包括但不限于:
- 含药组合产品
- III类植入器械
- 医美类产品
- 影像诊断类产品
Intertek凭借全球化的专家网络和对法规的精准洞察,已成为众多高端医疗器械企业攻克技术难关、赢得全球市场准入的坚实后盾。
关于驼人集团
驼人集团成立于1993年,以医疗器械为主业,涵盖医疗业务、国际业务、大健康业务和产业新城4大板块,是一家集研发、生产、销售、服务、文化于一体的现代化集团企业。现有5个生产基地,5个研发中心,拥有员工一万余人,其中研发团队、市场团队各两千余人并积极履行社会责任,安置残疾职工500余人。近年来,集团年销售收入达62亿元,展现出稳健的发展态势与行业引领力。
产品覆盖ICU、疼痛科、介入科等27个临床科室,涵盖耗材、中小型设备,拥有注册证501个(截止至2025年9月),产品品项四万余项,服务全国两万余家医院终端。主导产品麻醉包国内市场占有率48%,输注泵国内市场占有率36%。在中小型医疗设备领域,掌上超声、彩色超声诊断系统、血液透析设备、超声刀、视频喉镜等产品已成功上市并持续拓展。
自2006年启动国际化战略以来,驼人产品已出口至全球近百个国家和地区,在印度、肯尼亚、乌干达、坦桑尼亚、泰国、越南、尼日利亚、西班牙、巴西、巴基斯坦等国家设立子公司,具备完善的国际准入与供应链体系。
作为全球领先的质量与安全解决方案提供商,Intertek旗下瑞典公告机构IMNB(公告号NB 2862)已获得欧盟医疗器械法规(MDR, EU 2017/745)的官方授权。该机构的MDR授权范围广泛,覆盖有源医疗器械、无源医疗器械等不同风险等级的产品类别,能够为全球医疗器械制造商提供专业、合规的欧盟市场准入认证服务,助力企业高效满足欧洲市场法规要求。

Intertek审核及认证服务
- 医疗器械CE认证(包括EU MDR和UKCA)
- ISO13485:2016医疗器械质量管理体系 用于法规的要求
- MDSAP医疗器械单一审核程序
- 医疗器械质量管理体系及相关法规培训
- 二方审核
- 合规管理体系和人工智能AI管理体系
凭借100多个国家、1000多家实验室和分支机构及46000名员工的国际化网络和专业技术资源,Intertek为客户提供优质的本地化服务,助您更快获得全球市场准入通行证。
如果您有任何需求,请您联系所在地的办事处,或发送电子邮件至:
china.medical@intertek.com
关于Intertek天祥集团
Intertek是全球领先的全面质量保障服务机构,始终以专业、精准、快速、热情的全面质量保障服务,为客户制胜市场保驾护航。凭借在全球100多个国家的1,000多家实验室和分支机构,Intertek致力于以创新和定制的保障、测试、检验和认证解决方案,为客户的运营和供应链带来全方位的安心保障。
详情请登录:www.intertek.com.cn
